El lobby que no prosperó: Ministerio de Salud ratifica resolución que disminuye precio de medicamento que cura la Hepatitis C
31.08.2018
Hoy nuestra principal fuente de financiamiento son nuestros socios. ¡ÚNETE a la Comunidad +CIPER!
31.08.2018
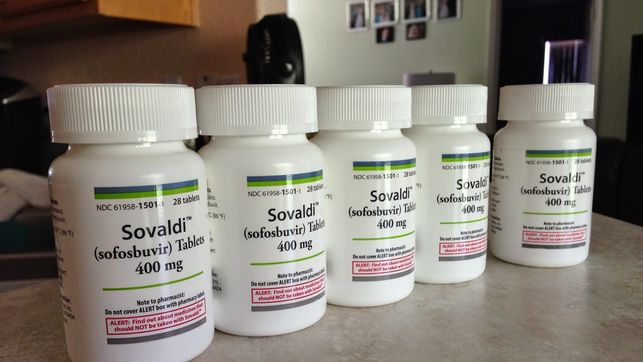
El ministro de Salud, Emilio Santelices, decidió ratificar la medida adoptada por su antecesora, Carmen Castillo, y seguir adelante con la demanda de una licencia obligatoria para los medicamentos que curan la Hepatitis C. Explicado en simple, esa decisión permite que el Estado o los ciudadanos puedan comprar esos remedios a un laboratorio distinto del que actualmente posee la patente en el país, el que al tener el monopolio de su venta, eleva excesivamente su precio. Actualmente la cura para la enfermedad puede llegar a costar $25 millones.
El laboratorio que posee la patente en Chile para distribuir el sofosbuvir, el medicamento que mezclado con otros cura la Hepatitis C, es Gilead, de origen estadounidense. En julio, CIPER reveló el intenso lobby que desplegó la industria de los laboratorios farmacéuticos para que el Ministerio de Salud echara pie atrás en su decisión. Ese lobby incluyó numerosas reuniones con personeros de los ministerios de Salud y Economía, visitas a embajadas de la Unión Europea y Estados Unidos, la presencia en Chile de un lobista norteamericano, y el intento por sumar a esa presión a
la CPC y a la Sofofa (vea aquí reportaje “Agresivo lobby de laboratorios contra resolución que baja millonario precio de medicamento”).
A la cabeza del lobby desplegado por los laboratorios estuvo Jean Jacques Duhart, vice presidente ejecutivo de la Cámara de Innovación Farmacéutica, ex subsecretario de Economía del primer gobierno de Michelle Bachelet.
El 28 de agosto el ministro Santelices firmó la Resolución 1.165, que ratifica una resolución anterior firmada por la ex ministra Castillo, y a la que el Laboratorio Gilead se opuso presentando en el Minsal un recurso de reposición. Ese recurso fue el que ahora rechazó Santelices. Eso permite que la solicitud de una licencia obligatoria para el medicamento que cura la Hepatitis C siga adelante.
El Ministerio de Salud (Minsal) consideró razones de salud pública para insistir con la demanda de una licencia obligatoria para el sofosbuvir: «La consideración de la Hepatitis C como un problema de salud pública, fue manifestada por este Ministerio de Salud sobre la base de las recomendaciones de la Organización Mundial de la Salud y sus agencias relacionadas (…) señalando que la progresión de la enfermedad puede causar complicaciones como cirrosis, hepatocarcinoma, trasplantes de hígado y hasta la muerte, con un alto costo social y económico para el país.
Misma consideración fue expresada por la Cámara de Diputados del Congreso Nacional», se lee en la resolución firmada por Santelices el 28 de agosto (ver aquí).
En esa resolución se afirma que el Minsal consideró que «los argumentos de Gilead no logran anular, opacar, o menoscabar dichas consideraciones». El laboratorio Gilead había argumentado ante el Minsal que una falta de acceso a medicamentos por consideraciones económicas «no constituye, en los hechos, una situación de extrema urgencia (…) Que en Chile hayan 1.058 pacientes en control con Hepatitis C y que 300 de ellos se encuentren en un estado avanzado de la enfermedad en ningún momento puede considerarse como una situación de riesgo inminente o de
peligro, que requiera la aplicación de una medida para afrontar una emergencia de salud pública». La respuesta del Minsal fue tajante: «El Ministerio de Salud tiene el deber de resguardar la salud pública, lo que significa proteger la salud tanto a la mayoría de la población, como a grupos minoritarios».
Las cifras oficiales de infectados pueden ser engañosas. Las estimaciones de los hepatólogos indican que existen alrededor de 50 mil personas infectadas con Hepatitis C en Chile, y que de ellas solo mil están diagnosticadas en el sistema público. Eso significa que poco más de un 2% de los infectados sabe el mal que padece.
El paso siguiente es la presentación de una demanda ante el Instituto Nacional de Propiedad Intelectual (Inapi) para que se emita una licencia obligatoria que permita la compra del sofosbuvir a otros laboratorios. Incluso la solución podría ser que el Estado desarrolle el medicamento, aunque es una opción menos probable. En caso que el Inapi acepte la demanda, deberá fijar su duración y alcance, limitarla a los fines para los que fue concedida y fijar el monto de la remuneración que se le pagará al titular de la patente. De todas formas, la decisión del Minsal es apelable ante la Corte de Apelaciones y luego ante la Corte Suprema.
El 20 de agosto, una semana antes de que se firmara la resolución, el Minsal modificó el decreto exento Nº 6, de 2010, para incluir a los enfermos de Hepatitis C (VHC) en la lista de quienes deben vacunarse obligatoriamente «contra enfermedades inmunoprevenibles». Desde el 1 de junio de 2018 se inició la vacunación contra Hepatitis A de todas las personas infectadas por VHC, diagnosticadas y confirmadas por el Instituto de Salud Pública.
En la modificación del decreto el Minsal argumenta que «la infección crónica por el VHC es una enfermedad que afecta a aproximadamente 184 millones de personas en el mundo, siendo una de las principales causas de cirrosis (27% de los casos), carcinoma hepatocelular (25% de los casos), así como de trasplante hepático». Agregó que «en Chile las enfermedades hepáticas determinan una proporción importante de la mortalidad general; particularmente las tasas de mortalidad por cirrosis en nuestro país son unas de las más altas del mundo. Mortalidad que es, proporcionalmente, mayor en el grupo etareo entre 45 y 59 años (…) las complicaciones como cirrosis hepatocarcinoma y trasplante de hígado representan un alto costo social y económico para el país, transformándose en un problema de salud pública», y que «la infección crónica por VHC es la causa más frecuenta de trasplante hepático adulto en nuestro país».